
敬畏生命,为爱发声
医疗无国界,健康伴您行

免费咨询电话
400 - 001 - 2811

在线人工客服
09:00 ~ 23:00

敬畏生命,为爱发声
医疗无国界,健康伴您行

免费咨询电话
400 - 001 - 2811

在线人工客服
09:00 ~ 23:00

别称Panobinostat
适应症帕比司他胶囊与硼替佐米及地塞米松联用,适用于既往接受过至少两种治疗方案(包含硼替佐米和一种免疫调节剂)的复发/难治性多发性骨髓瘤患者。
帕比司他是一种组蛋白去乙酰化酶抑制剂,与硼替佐米和地塞米松联合使用,适用于治疗接受过至少 2 种先前治疗方案(包括硼替佐米和一种免疫调节剂)的多发性骨髓瘤患者。该适应症是基于无进展生存期通过加速审批程序获批。该适应症的持续获批可能取决于确证性试验中对临床获益的验证和描述。
帕比司他
10mg、15mg、20mg
15mg:1号橙色胶囊,印有“LBH 15mg”。
20mg:1号红色胶囊,印有“LBH 20mg”。
胶囊:10mg:3号浅绿色胶囊,印有“LBH 10mg”。
24个月
储存温度为 20°C 至 25°C(68°F 至 77°F),允许在 15°C 至 30°C(59°F 至 86°F)之间波动。将泡罩包装存放在原装纸箱中,以避光。帕比司他 胶囊不应打开、压碎或咀嚼。应避免 帕比司他胶囊中的粉末与皮肤或粘膜直接接触。如果发生此类接触,请彻底清洗。
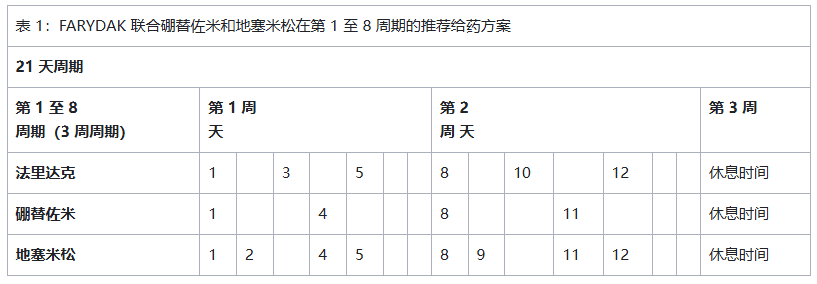
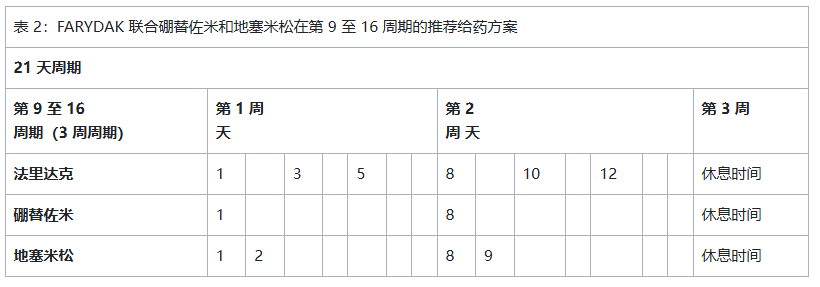
帕比司他的推荐起始剂量为 20mg,在每个 21 天周期的第 1 周和第 2 周,每隔一天口服一次,每周服用 3 剂,最多服用 8 个周期。对于有临床获益且未出现未缓解的严重或具有医学意义毒性的患者,可考虑再继续治疗 8 个周期。总治疗时长可能长达 16 个周期(48 周)。帕比司他 需与硼替佐米和地塞米松联合使用,具体用法见表 1 和表 2。
硼替佐米的推荐剂量为 1.3mg/m²,注射给药。地塞米松的推荐剂量为按计划服药日口服 20mg,需餐后服用。
临床研究中最常见的不良反应 (发生率至少为 20%) 是腹泻、疲劳、恶心、外周水肿、食欲下降、发热和呕吐。
最常见的非血液学实验室异常(发生率 ≥40%)是低磷血症、低钾血症、低钠血症和肌酐升高。最常见的血液学实验室异常(发生率 ≥60%)是血小板减少、淋巴细胞减少、白细胞减少、中性粒细胞减少和贫血。
尚不明确
接受 帕比司他 治疗的患者中,25% 出现严重腹泻]。接受帕比司他治疗的患者中,任何级别的腹泻发生率为 68%,而对照组为 42%。腹泻可在任何时间发生。在治疗前及治疗期间每周(或根据临床指示增加频率)监测患者的水合状态和血液电解质水平,包括钾、镁和磷酸盐,并进行纠正以预防脱水和电解质紊乱。腹泻一旦发作,应立即使用止泻药物。出现中度腹泻(每天 4 - 6 次大便)时,中断帕比司他治疗。确保开始使用帕比司他治疗的患者备有止泻药物。
接受帕比司他治疗的患者出现过严重和致命的心脏缺血事件、严重心律失常以及心电图(ECG)改变。接受帕比司他治疗的患者中,12% 发生心律失常,而对照组为 5%。接受 帕比司他 治疗的患者中,4% 发生心脏缺血事件,对照组为 1%。近期有心肌梗死或不稳定型心绞痛病史的患者,不应开始帕比司他治疗。
如果在使用帕比司他治疗期间,QTcF 增加至≥480 毫秒,应中断治疗,纠正任何电解质异常。若 QT 间期延长未缓解,则永久停用 帕比司他。
在治疗前进行心电图检查,并在治疗期间根据临床指示定期检查。在使用帕比司他治疗期间监测电解质,并根据临床指示纠正异常。
使用帕比司他治疗期间发生过致命和严重的出血事件。在复发多发性骨髓瘤的临床试验中,接受 帕比司他 治疗的患者有 5 例因出血事件死亡,而对照组为 1 例。这 5 例患者在事件发生时均有≥3 级血小板减少。帕比司他治疗组 4% 的患者报告出现 3/4 级出血,对照组为 2%。
帕比司他可导致骨髓抑制,包括严重的血小板减少、中性粒细胞减少和贫血。在治疗前进行基线全血细胞计数(CBC),并在治疗期间每周监测 CBC(或根据临床指示增加频率)。对于骨髓抑制,建议调整剂量。由于 65 岁以上患者骨髓抑制的发生频率更高,因此应对这些患者更频繁地监测 CBC。
服用帕比司他的患者报告发生过局部和全身感染,包括肺炎、细菌感染、侵袭性真菌感染和病毒感染。接受 帕比司他 治疗的患者中,31% 发生严重感染(包括 10 例死亡),对照组为 24%(包括 6 例死亡)。所有级别的感染在两组中的发生率相似。有活动性感染的患者不应开始 帕比司他 治疗。在治疗期间监测患者是否有感染的体征和症状;如果确诊感染,应立即进行适当的抗感染治疗,并考虑中断或停用帕比司他。
接受帕比司他治疗的患者出现过肝功能障碍,主要表现为转氨酶和总胆红素升高。治疗前及治疗期间应定期监测肝功能。如果观察到肝功能检查异常,可考虑调整剂量,并对患者进行随访,直至指标恢复正常或达到治疗前水平。
孕妇使用帕比司他可导致胎儿伤害。帕比司他对大鼠和兔子具有致畸性。如果在怀孕期间使用帕比司他,或者患者在服用帕比司他期间怀孕,应告知患者药物对胎儿的潜在危害。
建议有生殖潜力的女性在服用帕比司他期间避免怀孕。建议有生殖潜力且有性生活的女性在服用 帕比司他 期间及最后一剂帕比司他后至少 3 个月内采取有效的避孕措施。
建议有性生活的男性在治疗期间及最后一剂帕比司他后 6 个月内使用避孕套。
孕妇使用帕比司他可导致胎儿伤害。帕比司他对大鼠和兔子具有致畸性。如果在怀孕期间使用 帕比司他,或者患者在服用本药期间怀孕,应告知患者药物对胎儿的潜在危害。
尚不清楚帕比司他是否会随人类乳汁排出。由于许多药物会随人类乳汁排出,并且考虑到哺乳婴儿可能发生严重的药物不良反应,应根据药物对母亲的重要性,决定是停止哺乳还是停止用药。
在大鼠的胚胎 - 胎儿发育研究中出现了包括畸形在内的胚胎 - 胎儿毒性。在开始使用帕比司他治疗前以及治疗期间,应对有生育潜力的女性进行妊娠检测。
女性:帕比司他可导致胎儿伤害。建议有生殖潜力的女性在服用 帕比司他 期间避免怀孕。建议有生殖潜力且有性生活的女性在服用 帕比司他 期间及最后一剂 帕比司他 后至少 3 个月内采取有效的避孕措施。建议患者在服用 帕比司他 期间,如果怀孕或怀疑怀孕,应联系医疗保健人员。
男性:建议有性生活的男性在治疗期间及最后一剂帕比司他后至少 6 个月内使用避孕套。
帕比司他在儿童中的安全性和有效性尚未确立。
在帕比司他治疗多发性骨髓瘤的临床试验中,42% 的患者年龄在 65 岁及以上。
65 岁及以上的患者发生某些不良事件的频率更高,因不良事件停药的频率也更高。在 65 岁及以上的患者中,与疾病进展无关的死亡率为 9%,而 65 岁以下的患者为 5%。
在复发多发性骨髓瘤的随机临床试验中,未观察到老年患者与年轻患者在疗效上有重大差异。在 帕比司他 治疗组中,65 岁及以上的患者因不良反应导致永久停药的发生率为 45%,而 65 岁以下的患者为 30%。应更频繁地监测 65 岁以上患者的毒性反应,尤其是胃肠道毒性、骨髓抑制和心脏毒性。
尚未评估帕比司他在肝功能损害患者中的安全性和有效性。
在一项药代动力学试验中,轻度(胆红素≤1 倍正常上限且 AST>1 倍正常上限,或胆红素>1.0 - 1.5 倍正常上限且任何 AST 水平)或中度(胆红素>1.5 - 3.0 倍正常上限,任何 AST 水平)肝功能损害(NCI - ODWG 标准)的患者,帕比司他的 AUC 分别增加 43% 和 105%。轻度或中度肝功能损害患者应降低 帕比司他 的起始剂量。严重肝功能损害患者避免使用。应频繁监测肝功能损害患者的不良事件。
轻度 [肌酐清除率(CrCl)≥50 - <80mL/min] 至重度肾功能损害(CrCl <30mL/min)对帕比司他的血浆暴露量没有影响。尚未在终末期肾病(ESRD)患者或透析患者中研究 帕比司他。帕比司他是否可透析尚不清楚。
帕比司他是 CYP3A 的底物,并且抑制 CYP2D6。帕比司他还是 P - 糖蛋白(P - gp)转运系统的底物。
CYP3A 抑制剂:与单独使用 帕比司他 相比,帕比司他 与强效 CYP3A 抑制剂合用,帕比司他的 Cmax(血药浓度峰值)和 AUC(药时曲线下面积)分别增加 62% 和 73%。
与强效 CYP3A 抑制剂(如波普瑞韦、克拉霉素、考尼伐坦、茚地那韦、伊曲康唑、酮康唑、洛匹那韦 / 利托那韦、奈法唑酮、奈非那韦、泊沙康唑、利托那韦、沙奎那韦、特拉匹韦、泰利霉素、伏立康唑)合用时,将剂量减至 10mg。告知患者避免食用杨桃、石榴或石榴汁、葡萄柚或葡萄柚汁,因为已知这些食物会抑制 CYP3A 酶。
CYP3A 诱导剂:尚未在体外或临床试验中评估 帕比司他 与强效 CYP3A 诱导剂合用的情况,但帕比司他的暴露量可能会降低。使用机制模型进行的模拟显示,在存在强效 CYP3A 诱导剂的情况下,帕比司他的全身暴露量大约降低 70%。因此,应避免同时使用强效 CYP3A 诱导剂。
CYP2D6 底物:帕比司他 使 CYP2D6 敏感底物的中位 Cmax 和 AUC 分别增加约 80% 和 60%,但存在很大差异。避免 帕比司他 与 CYP2D6 敏感底物(如托莫西汀、地昔帕明、右美沙芬、美托洛尔、奈必洛尔、奋乃静、托特罗定和文拉法辛)或治疗指数较窄的 CYP2D6 底物(如硫利达嗪、匹莫齐特)合用。如果无法避免同时使用 CYP2D6 底物,应频繁监测患者的不良反应。
不建议同时使用抗心律失常药物(包括但不限于胺碘酮、丙吡胺、普鲁卡因胺、奎尼丁和索他洛尔)以及其他已知会延长 QT 间期的药物(包括但不限于氯喹、卤泛群、克拉霉素、美沙酮、莫西沙星、苄普地尔和匹莫齐特)。对于有已知 QT 间期延长风险的止吐药,如多拉司琼、昂丹司琼和托烷司琼,在频繁进行心电图监测的情况下可以使用。
药物过量的经验有限。预计会出现临床试验中观察到的不良反应加剧,包括血液学和胃肠道反应,如血小板减少、全血细胞减少、腹泻、恶心、呕吐和厌食。监测心脏状况,包括心电图,并评估和纠正电解质紊乱。对于血小板减少性出血,可考虑输注血小板。目前尚不清楚帕比司他是否可透析。
帕比司他的绝对口服生物利用度约为 21%。在晚期癌症患者中,口服给药后 2 小时内(达峰时间 Tmax)可观测到帕比司他的血药浓度峰值。在给药剂量范围内,帕比司他的血药浓度峰值(Cmax)和药时曲线下面积(AUC)大致呈剂量比例增加。
36 名晚期癌症患者在高脂餐后 30 分钟口服 帕比司他,与空腹状态相比,血浆中帕比司他的 Cmax 和 AUC₀₋₄₈分别降低约 44% 和 16%。这些患者的中位 Tmax 也延迟了 2.5 小时。
帕比司他的水溶性取决于 pH 值,pH 值越高,溶解度越低。帕比司他与升高胃 pH 值的药物联合使用的情况尚未在体外或临床试验中进行评估;不过,利用基于生理药代动力学(PBPK)模型进行模拟时,未观察到帕比司他吸收发生改变。
在体外,帕比司他与人体血浆蛋白的结合率约为 90%,且与浓度无关。帕比司他是 P - 糖蛋白(P-gp)的底物。
帕比司他广泛代谢。其生物转化涉及的相关代谢途径包括还原、水解、氧化和葡萄糖醛酸化过程。经 CYP3A 代谢的部分约占肝脏中帕比司他总消除量的 40%。在体外,CYP2D6 和 CYP2C19 途径的贡献较小。在体外,UGT1A1、UGT1A3、UGT1A7、UGT1A8、UGT1A9 和 UGT2B4 参与了帕比司他的葡萄糖醛酸化。
本网站不销售任何药品,只做药品信息资讯展示 鲁ICP备2023035557号-5 证书编号:(鲁)-经营性-2022-0196 找药网 找药助手